# BeCl_2 # e # TeCl_2 # são moléculas covalentes, mas # BeCl_2 # é linear enquanto # TeCl_2 # é dobrado. Por quê?
#"TeCl"_2#: A Central #"Te"# átomo tem #6# elétrons de valência. Quando os dois #"Cl"# átomos se ligam ao átomo central, cada um deles contribui com um elétron para formar dois ligações sigma. Isso deixa #4# elétrons nos átomos centrais na forma de #2# pares de elétrons solitários.
Este é o VSEPR forma #"AX"_2"E"_2#, uma forma de tetraedro com dois pares de elétrons e dois átomos, criando uma forma molecular dobrada.
![]()
#"BeCl"_2#por outro lado, tem #"Be"# como seu átomo central. Desde a #"Be"# só tem #2# elétrons de valência, as duas ligações sigma formadas pelo #"Cl"# átomos deixam #"Be"# sem pares solitários.
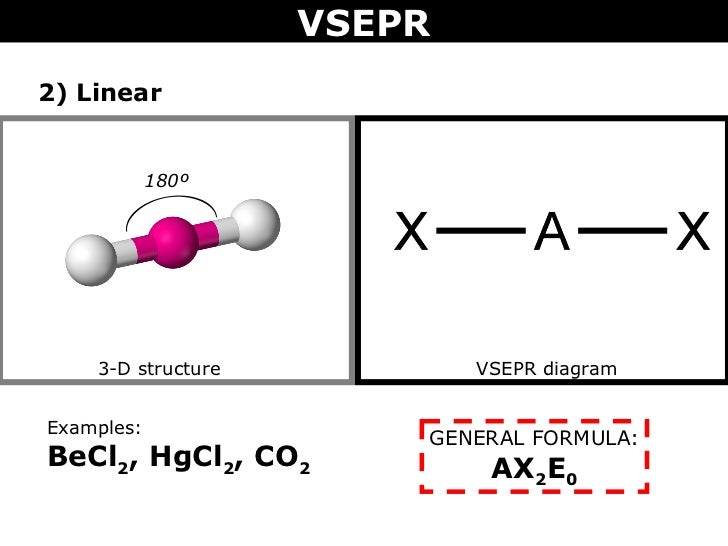
A forma VSEPR é #"AX"_2"E"_0# e forma uma forma linear.