Qual é a polaridade da ligação do CH4?
Responda:
O momento dipolar de um #"C-H"# vínculo é provavelmente 0.34 D.
Explicação:
Costumamos dizer que um #"C-H"# A ligação é não polar porque as eletronegatividades de #"C"# e #"H"# estão tão perto um do outro.
No entanto, os valores são #"C = 2.55"# e #"H = 2.20"#.
A diferença corresponde ao caractere iônico 3%, portanto, um #"C-H"# A ligação deve ter um pequeno momento dipolar.
Das intensidades experimentais de IR do metano, podemos inferir que #µ_text(C-H) = "0.34 D"#dirigido #stackrelcolor(blue)(δ⁻)("C")"-"stackrelcolor(blue)(δ⁺)("H")#.
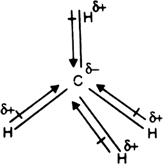
Os cálculos teóricos fornecem resultados variados, mas a maioria dos valores experimentais está entre 0.3 D e 0.4 D.

