Qual é a polaridade da ligação do h2o?
Polaridade da ligação refere-se à separação de carga dentro de uma ligação.
Ligações entre átomos de diferentes eletro-negatividade são polares. O átomo mais eletronegativo tem uma maior densidade of ligação elétrons ao seu redor, dando-lhe uma carga negativa parcial (δ⁻). O átomo menos eletronegativo retira parte de sua densidade de elétrons, dando-lhe uma carga positiva parcial (δ⁺).
Na água, a separação de carga nas ligações OH é devida às diferentes eletronegatividades de oxigênio e hidrogênio. Como o oxigênio é mais eletronegativo que o hidrogênio, uma ligação OH é covalente polar. Cada ligação OH é covalente polar com uma carga negativa parcial no átomo de oxigênio.
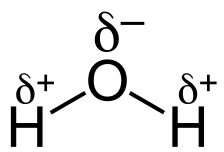
A polaridade nas ligações também é mostrada por uma seta representando um dipolo (duas cargas separadas por uma distância). Há um sinal de + na cauda da seta. A ponta da seta aponta o sinal + em direção ao átomo δ⁻. Assim, a água tem dois dipolos de ligação OH, cada um dos quais aponta para o átomo O.


